细胞是生物体基本的结构和功能单位,但病毒只有蛋白质外壳包裹着紧凑的核酸物质(DNA或RNA),并不具备完整的细胞结构。所以对于病毒而言,想要存活就必须寄生在宿主细胞中,并且借助宿主细胞的核苷酸和氨基酸来合成自身的一些组件,完成自己的基因组复制、蛋白质外壳制造,以及组装完整的新病毒。
在这个过程中,人们理所当然地认为,完整的病毒基因组只能同时感染一个宿主细胞,并在其中完成新病毒的复制、组装和释放。然而,最近eLife上发表的一项新研究颠覆了这一传统认知。
正如来自法国蒙彼利埃大学研究人员发现的那样,一些病毒不仅可以分成多个部分,分别感染宿主细胞,而且这些基因组分裂的病毒可以像拆散的拼图一样,分散在多个宿主细胞中蓬勃生存,然后这些在不同细胞中复制的病毒粒子,自我组装成新的完整病毒并继续感染。

图 | 法国国家农业研究所的植物病理学家Anne Sicard(左)及其同事(右)
本次新研究的作者、法国蒙彼利埃大学和法国国家农业研究所(INRA)植物病理学家Anne Sicard表示,病毒学中的经典观点认为病毒复制周期发生在单个细胞内,但对于她和她的团队研究的多分区病毒(multipartite virus)来说,似乎并非如此,这些病毒的多个粒子独立感染细胞,并在植物宿主细胞中独立地复制。
分开感染的病毒基因组多分区病毒已有半个多世纪的历史,当时的研究人员意识到病毒可以由两个或两个以上独立的部分组成,而且每一个独立的部分对于病毒感染都至关重要。例如,多分区病毒其中的一部分可能是制造关键酶所必需的,而另一部分则是制造包装并转运病毒粒子的外壳所必需的。
但是,病毒为什么要把它的基因组分开呢?毕竟,将每一部分都很重要的基因组分成不同的部分,存在着相当大的风险,比如基因组的某些部分很容易丢失或组装时落下,如果整个基因组的一部分丢失,那么剩下的基因组也基本就完蛋了。
科学家们在发现多分区病毒后也感到十分疑惑,“为什么病毒会这样做呢?为什么要分开基因组?将这些片段单独包装有什么好处?” 荷兰生态学研究所的进化病毒学家Mark P. Zwart表示。
为了探索这些问题,研究人员曾开发模型来预测这种多分区的方式,将在什么情况下从一个更典型的病毒祖先进化而来,所有这些理论都建立在假设所有的病毒片段必须同时感染一个细胞的基础上。
但结果很令人困惑。2012年的一项研究得出结论,无论病毒基因组多分区的好处是什么,缺点都是如此之大,以至于不可能存在超过四个分段的病毒。然而,已知一些多分区病毒,如蚕豆坏死萎蔫病毒(FBNSV)有多达八个基因组片段,每个片段都由不同的病毒粒子所携带。从理论上讲,它不可能进化得来,但又如何解释它的存在?

图 | FBNSV导致的植物症状(Journal of Virology )
在这项最新研究中,INRA的植物病毒学家认为,人们对于病毒学的一些理论假设肯定在哪里搞错了。因此,研究人员决定对其中的关键假设——即所有病毒的基因组必须同时进入同一个细胞才会发生感染——进行验证。以前之所以没有人提出质疑,是因为所有人都理所当然地认为这些多分区病毒的基因组片段必须在一起。
当研究人员仔细观察FBNSV感染过程时,果然发现了其中的“异常”。通过使用不同颜色的荧光探针同时标记两个病毒粒子,研究小组发现在他们检测的绝大多数单个寄主植物细胞中,病毒基因组片段是缺失的。此外,研究人员还发现病毒复制所需的蛋白质存在于没有基因组编码片段的细胞中。
由此,研究人员推断,病毒粒子必须在细胞之间共享基因产物——信使RNA或蛋白质,以便每个粒子都可以独立复制,并将自身包装成粒子以进行传播和再次感染。
但在植物宿主细胞中,病毒所必需的基因产物是如何共享的,研究人员目前还不完全清楚。
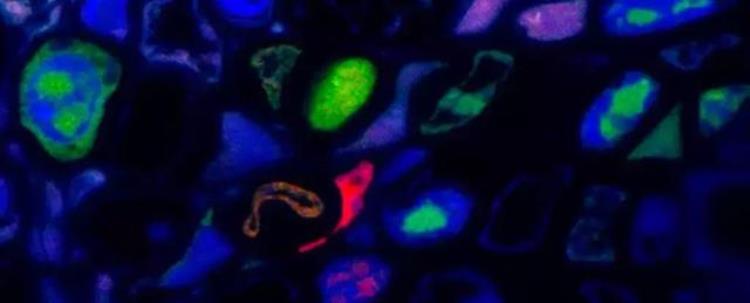
图 | 存在于不同细胞的病毒基因组片段(来源:eLife)
这个新发现,解释了多分区病毒如何在植物体内维持感染,并揭示了一个关于病毒如何传播的新秘密。例如,FBNSV寄宿于吃蚕豆植物的蚜虫来传播自己,这些小昆虫必须一次性捕获FBNSV的所有八个病毒粒子,并将它们引入同一植物才能成功传递感染,但是据推测,大部分感染过程都没有成功,因为蚜虫只捕获了八个病毒粒子中的一部分。
这也就部分解释了宿主内部的问题,因为病毒粒子不必一起到达所有细胞,但在宿主之间传播仍然存在难以解释的问题。
病毒学新认知为什么病毒会从多分区的感染方式中受益,仍然值得探究。
研究人员提出一个想法,认为基因组的划分允许每个片段在不同频率上发生变化,这是一种应急的调节基因表达的方式,因为一个特定基因的活性水平可能取决于它在细胞中的复制数量。每次病毒感染一个新的宿主,片段的频率就会发生变化,这可以让病毒测试在新的细胞环境中基因表达的最佳程度。
美国坦帕大学的病毒学家Eric Freundt推测,如果宿主植物的先天防御仅破坏那些表达某些病毒蛋白的细胞,那么将病毒蛋白质的基因分布到不同的粒子中,可能会保证病毒在某些细胞中不被发现。Freundt认为,另一种可能性是,如果病毒一次性产生所有蛋白质,可能会导致宿主细胞超负荷工作,并“累死”细胞。通过将其基因组分布在许多植物细胞中,病毒可以避免压垮任何单个寄生的细胞。
果真如此,这些病毒似乎本能地避免把鸡蛋放在一个篮子里。
不过,研究人员仍指出,以上这些只是假设,多分区病毒的演变原因仍然很神秘。
Zwart指出,关于多分区优势的大多数想法都是关于基因组分割,而不是将病毒划分为不同的感染单位。将基因组分成区段,允许病毒更容易地重组其基因的各种有利形式。
亚利桑那州立大学的病毒学家Arvind Varsani对此表示赞同,“从模块化的角度来看,你可以看到多分区病毒的优势,每个模块都可以独立,病毒可以更快地获得每个模块,并通过混合和匹配来适应新环境。”

(来源:Quanta Magazine)
这种假设的最有力证明就体现在流感病毒中,流感病毒简直是病毒重组大师。流感病毒基因组也有八个片段,尽管这些片段在一个病毒外壳中包装在一起,这使它既能够获得多分区的好处,又不用承受多分区的全部代价。
而且流感病毒可能比第一眼看上去更像FBNSV病毒。伊利诺伊大学香槟分校的病毒学家 Christopher Brooke发现,根据病毒株的不同,只有一小部分(1%-10%)流感病毒粒子含有全部八个基因组片段的功能性拷贝。
“绝大多数流感病毒粒子都是不完整的,或者称之为半传染性粒子,即它们本身无法自行启动有效复制,”他解释道,“这是一个惊喜,因为它表明这种超级成功且具有高度传染性的病毒,主要存在于这些不能自行复制的粒子中。”
Brooke还预测,探究病毒如何作为群体而不是单个病毒粒子运作,最终将成为许多不同病毒系统的关键。
这种重要性就体现在概念上,目前将任何单个病毒粒子内的DNA视为其基因组的定义,可能过于局限。相反,把病毒基因组想象成整个病毒种群的一组基因可能更恰当。而理论家们已经在深入研究其中的影响。
Zwart也预计,很快就会出现新的理论模型来探索这些见解,例如使用多层次的自然选择方式来描述这些病毒的进化。在一个单独的宿主植物中,自然选择的局部力量将使病毒成功地平衡其片段的产率。但是当病毒转移到新宿主植物时,它必须要能够适应新的宿主环境,因此需要保留一些适应性。这个时候,更高层次的自然选择可能会调节局部并更均匀地重新平衡分区的比例。
Zwart说,“这一动态过程如此多样,真的很吸引人。”

韩国发现首例新冠重组毒株XL感染病例,新冠病毒为何会发生重组?
韩国发现首例新冠重组毒株XL感染病例,新冠病毒为何会发生重组?下面就我们来针对这个问题进行一番探讨,希望这些内容能够帮到有需要的朋友们。
新冠病毒变异,再生曲折。最先是韩国,初次发现了奥密克戎新重组毒株XL传染病例,诊断病例已注射完三剂新冠疫苗;此外,日本国内也首度发现了新冠重组毒株XE传染病例;更不容乐观的是英国,新冠重组毒株XE传染病例数已经飙涨,据英国卫生安全局的最新的数据统计,截止到4月5日,英国已发现1125例XE毒株传染病例,相比于3月25日的637例提升近一倍。
此外,日本忽然传来新冠疫情警报。4月11日,日本媒体报导称,因奥密克戎BA.2毒株的快速扩散,造成日本全国各地多地新冠传染总数创厉史新纪录,或迈入迄今为止最规模性的第七波新冠新冠疫情。此外,据英国国家统计局的最新数据表明,奥密克戎BA.2毒株已经英格兰地区迅速散播,造成3月至今55岁以上人群患病率猛增,比之前平均超出20倍。英国权威专家警示称,较年老人员发生危重或死亡的风险性更高一些,英国恐迈入新一波住院治疗和死亡高峰期。
奥密克戎基因变异毒株的高传播性,令全世界传染总数猛增,从而致使了全世界再度发生一波致死人数高峰期,有关#奥密克戎时兴期内全世界死亡率再发生高峰期#的话题讨论,也一度冲到微博热搜。
持续基因变异的新冠病毒感染,仍然难以相信。4月12日,一则有关#韩国发现第一例新冠重组毒株XL传染病例#的话题讨论,冲到微博热搜首,阅读量超2.6亿。
4月12日,中央新闻引用韩国中央疫防防范措施总部报导,韩国初次在地区发现奥密克戎新重组毒株XL传染病例,现阶段已经对该病例开展实验室检测。该诊断病例已注射完三剂新冠疫苗,于3月23日诊断,现阶段暂时没有症状的。
XL毒株是至今发现的17种重组毒株(XA-XS)的在其中之一,由“奥密克戎”初始株BA.1和乳头瘤病毒株BA.2重组而成。韩国疾病预防单位表明,世卫组织将XL归到奥密克戎类毒株,预估其性能不容易发生很大转变。由于现阶段未有有关其传播力、致危重症率等数据的材料,防疫部门将加强对基因变异株的监测工作中。
此外,日本也首度发生了新冠重组毒株XE病例,据日本厚生劳动省表明,日本国内初次确定新冠重组毒株XE传染病例,诊断病例为一名30几岁的女士,她于3月26日自美国抵达日本成田机场,在飞机场的检疫所内接纳的新冠检验呈阳性,后经进一步分析,最后确定其传染的是新冠重组毒株XE。
更不容乐观的是英国,新冠重组毒株XE传染病例数已经飙涨。据英国卫生安全局的最新的数据统计,截止到4月5日,英国已发现1125例XE毒株传染病例,相比于3月25日的637例提升近一倍。代表着,XE毒株在英国已发生了小区散播扩张的征兆。
新冠毒株XE最开始是在2022年1月19日在英国被发现,该病毒感染已散播长时间。据英国卫生安全局(UKHSA)的技术性简讯详细介绍,XE是一种奥密克戎BA.1与BA.2的重组体,该重组体的绝大多数基因归属于BA.2的S遗传基因。
接着在泰国、印度、以色列及其中国香港和台湾地区都陆续发现了传染XE毒株的诊断病例。有关XE毒株的传播力,英国的初始科学研究数据显示,XE重组体的快速传播比奥密克戎BA.2基因变异株高9.8%。此外,世界卫生组织在近期的报告书中表明,XE毒株可能是目前为止已经知道极具感染性的毒株。
世界卫生组织公布的最新一期新冠新冠疫情周刊强调,新冠病毒感染仍在再次演变,由于现阶段其在全世界范畴内的高质量散播,新冠病毒感染有可能会再次发生越来越多的基因变异毒株,包含重组毒株。
实际上,XE并非第一个被发现的重组毒株。新冠疫情爆发至今,新冠重组毒株的产生并不少见,但绝大部分重组毒株因在传播方式上并不具备优越性而慢慢当然衰落。
研究发现,新基因变异株更够替代旧毒株必须与此同时具有2个标准,新基因变异株要具备更强的散播工作能力,且可以肇事逃逸旧毒株产生的免疫力。目前为止,全部权威性的探究结论都确认,奥密克戎BA.2基因变异株快速传播显著更强,且与BA.1不一样的免疫逃逸。
韩国发现了首例新冠重组毒株XL感染病例,这种重组病毒有什么特点?
这种重组病毒的特点是传播性要比之前的更强。
据韩联社昨晚报道,韩国中央防疫对策本部4月12日正式确认首例新冠肺炎重组株“XL”病例,目前防疫部门正在进行流行病学调查。韩国方面表示,该患者自3月23日检测呈阳性,但已接种3针疫苗,目前无明显症状。很多人听到“XL”会觉得奇怪。我们不妨理解为“XE菌株的姐妹”。XE variant作为OmicronBA.1原毒株和BA.2亚种毒株的组合,完美结合了两种毒株的特性,比BA.2亚种快10%,比原毒株BA.1快1.4倍。
XL株是迄今发现的17个重组株之一,与最近在十几个国家发现的XE株相似。它是Omicron的原始菌株BA.1和亚型菌株BA.2的重组合成。到目前为止,还没有关于XL株传播特性的资料,只在英国发现过。据韩国疾控部门称,世卫组织将XL株列为Omicron株,预计其特性不会有大的变化。目前还没有关于其传播力、重症率等信息。,防疫部门表示将加强对变异菌株的监测。XL病毒是新发现的病毒,目前研究的还不多。根据韩国相关部门的描述,XL株是由冠病变株Omicron原始株BA.1和亚型变异株BA.2重组而成,估计其特性不会有大的变化。相信很快,韩国就会公布其传播力、重症率等信息。
英国卫生安全局称,如果一个人同时感染了两种或两种以上的变异毒株,这些毒株的遗传物质会在感染者体内混合,出现重组毒株。世卫组织称,由于新冠肺炎的演变,包括重组菌株在内的新突变菌株的风险仍然很高。






